Введение
Это руководство предназначено для руководителей отделов закупок, основателей брендов и менеджеров по соблюдению нормативных требований, занимающихся поставками зубной пасты, ополаскивателей для рта и отбеливающих средств, и отвечающих за утверждение и размещение на полках товаров для ухода за полостью рта. Аудиты и соблюдение нормативных требований в отношении средств по уходу за полостью рта являются основными причинами задержек запуска, таможенных задержек, затрат на перемаркировку и неудач в привлечении розничной торговли — а не качество рецептуры.

Уход за полостью рта Более строгий контроль, чем в случае с обычной косметикой, обусловлен наличием активных ингредиентов, заявленными свойствами и отслеживаемостью партий, а четырехнедельная задержка на таможне может заблокировать поступление шестизначных сумм от минимального объема заказа. В этой статье подробно рассматривается логика региональных проверок, специфические требования к средствам по уходу за полостью рта и четко определены обязанности OEM-производителей и импортеров.
В Оралабкс, Мы работаем с брендами именно на этом этапе, когда формула продукта готова, но от соблюдения нормативных требований зависит, выйдет ли товар на рынок.
Как на самом деле работают проверки состояния полости рта (обязательные и необязательные)
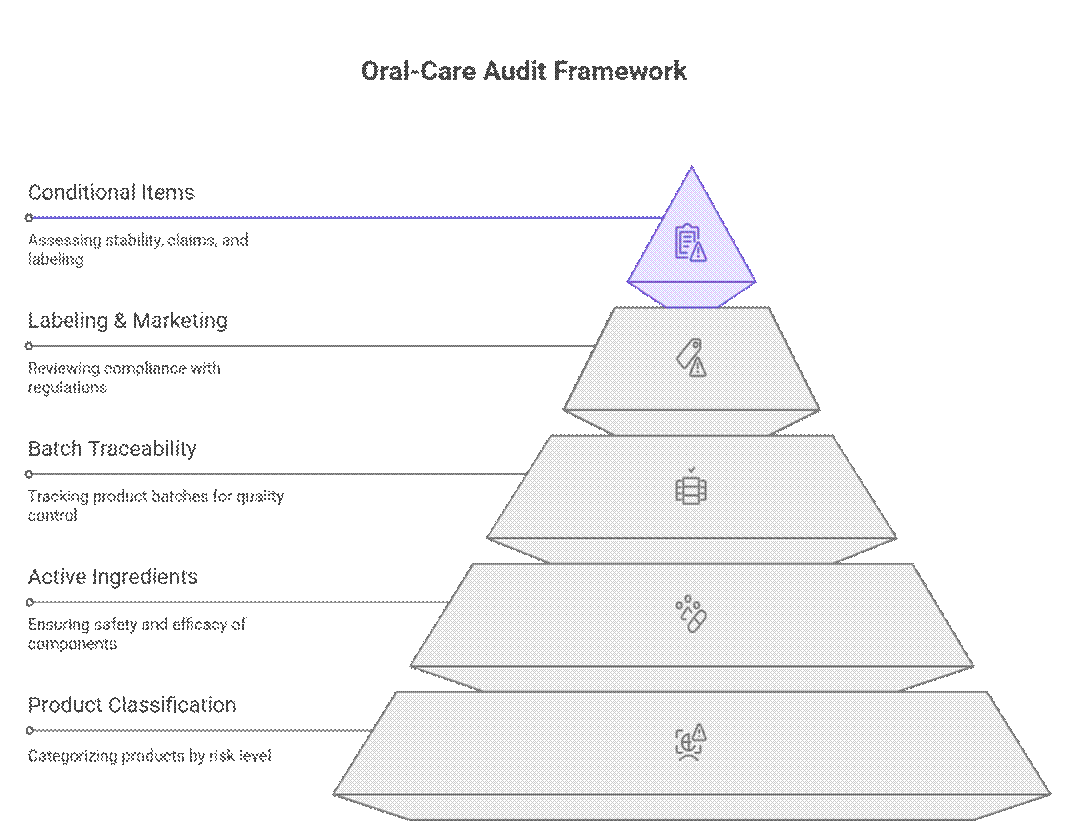
Регуляторы проводят аудит и проверку соответствия продукции для ухода за полостью рта, используя многоуровневую систему оценки рисков, которая отдает приоритет классификации продукции, активным ингредиентам и отслеживаемости партий до рассмотрения вопроса о маркировке или выходе на рынок. Только после прохождения этих этапов они рассматривают условные пункты, такие как продолжительность стабильности, обоснованность заявлений или переходная маркировка.
Что аудиторы проверяют в первую очередь (не подлежит обсуждению)
Аудиторы начинают с четкого набора требований, которые должны быть выполнены, прежде чем можно будет приступить к дальнейшей проверке.
- Классификация продукции (косметические средства против безрецептурных препаратов / квазилекарственных средств)
Неправильная классификация остается одним из наиболее распространенных нарушений требований к аудиту зубных паст, особенно когда производители неправильно понимают пороговые значения классификации средств по уходу за полостью рта как косметических и безрецептурных, связанные с активными веществами и заявлениями о свойствах.
- Пороговые значения активных ингредиентов
Проверяет соответствие ограничениям по содержанию таких ингредиентов, как фторид или хлорфенол, что может привести к контролю за отпускаемыми без рецепта лекарствами или к нарушениям на уровне отдельных препаратов.
- Регистрация производителя и статус GMP
Обеспечивает надлежащую регистрацию производственного предприятия OEM и его работу в соответствии с утвержденными стандартами GMP. производство средств по уходу за полостью рта.
- Отслеживаемость партий и готовность к отзыву продукции
Подтверждает наличие полных записей о партиях продукции для отслеживания, изоляции и быстрого отзыва продукции по требованию регулирующих органов или розничных продавцов.
Что является условным требованием?
Помимо обязательных требований, аудиторы применяют риск-ориентированный анализ к документации и результатам тестирования. Применение этих требований варьируется в зависимости от рыночных и продуктовых рисков, но пробелы часто приводят к задержкам или условному одобрению.
- Длительность стабильности (ускоренное и реальное время)
Ускоренная проверка стабильности может быть достаточной для ранних или низкорисковых запусков, но для продуктов с активными веществами, длительным сроком хранения или более строгими требованиями рынков, таких как ЕС или страны Персидского залива, часто требуется проверка стабильности в реальном времени. Крупные производители оборудования проводят проверку стабильности в реальном времени параллельно.
- глубина обоснования утверждения
Для подтверждения основных косметических свойств обычно требуется минимальное обоснование, в то время как для подтверждения эффективности необходимы лабораторные или клинические данные. Аудиторы отмечают заявления, которым не хватает доказательств или которые не соответствуют окончательной рецептуре.
- Местный язык и форматы маркировки
Для проверки могут подойти этикетки на английском языке, но для окончательного утверждения обычно требуется маркировка на местном языке, соответствующая требованиям. Аудиторы часто отмечают отсутствие дополнительных этикеток, неверные названия ингредиентов или рискованные переводы утверждений.
Что подлежит обсуждению (с крупным производителем оригинального оборудования)?
Хотя правила кажутся жесткими, опытные аудиторы понимают практические реалии производства. При наличии проверенного OEM-производителя и четкого плана соблюдения требований некоторые требования могут быть введены поэтапно или последовательно, не препятствуя выходу на рынок.

- Переходная маркировка
Аудиторы могут принять промежуточную маркировку для первых партий, если окончательный макет утвержден и запланирован. Крупные производители оригинального оборудования (OEM) обеспечивают разделение партий и не допускают попадания в розничную продажу неокончательных этикеток.
- Поэтапная разработка документации в процессе масштабирования.
Аудиторы могут принять промежуточную маркировку для первых партий, если окончательный макет утвержден и запланирован. Крупные производители оригинального оборудования (OEM) обеспечивают разделение партий и не допускают попадания в розничную продажу неокончательных этикеток.
- Параллельное тестирование во время пилотных запусков
Крупные производители оригинального оборудования проводят испытания на стабильность, микробиологическую безопасность и качество упаковки в ходе пилотных партий, сокращая сроки запуска на недели или месяцы.
Визуальный шаблон #1: Иерархия требований аудита (средства по уходу за полостью рта)
| Уровень приоритета аудита | Категория требований | Что это включает | Влияние аудита в случае отсутствия информации |
| Уровень 1 — Не подлежит обсуждению | Классификация продукции | Определение косметических и безрецептурных препаратов / квазилекарственных средств, пороговые значения активного ингредиента | Немедленный провал аудита или задержка на таможне |
| Статус GMP и производственных мощностей | ISO 22716, регистрация в FDA, гигиенический контроль. | Отказ от партии товара, дисквалификация фабрики. | |
| Прослеживаемость партий | Протоколы партий, готовность к отзыву продукции, кодирование партий. | Обязательные корректирующие действия, возможный отзыв продукции. | |
| Уровень 2 — Требуется при определенных условиях | Поддержка стабильности | Ускоренная и/или стабильная в режиме реального времени, привязанная к сроку годности. | Условное одобрение, обязательства после выхода на рынок. |
| Обоснование утверждения | Данные, подтверждающие эффективность отбеливания, фторирования, удаления зубного налета и применения CPC. | Требуется удаление или перемаркировка заявки. | |
| Соответствие местным требованиям к маркировке | Язык, формат, правила именования ингредиентов | Затраты на перемаркировку, задержка запуска. | |
| Уровень 3 — Обсуждаемо (зависит от производителя) | Переходная маркировка | Временные макеты с утвержденными окончательными версиями в архиве. | Принято с документально оформленным планом прекращения действия. |
| Поэтапная документация | Отложенные долгосрочные испытания на этапе масштабирования. | Принимается при условии проведения оценки рисков и планирования. | |
| Параллельное тестирование | Испытания на стабильность и микробиологическую целостность в ходе пилотных испытаний. | Принимаются с жестким контролем качества партий. |
Вывод от производителя:
Бренды не проходят аудиты, рассматривая пункты 2-го и 3-го уровней как необязательные предположения, а не как управляемый риск. Надежный производитель оригинального оборудования (OEM) активно контролирует эту иерархию.
Пункты аудита, касающиеся ухода за полостью рта, которые бренды не упомянули.
Большинство случаев провала проверок качества средств по уходу за полостью рта происходит не из-за отсутствия сертификатов. Они возникают, когда производители применяют общие косметические предположения к продуктам с более высоким риском, содержащим активные ингредиенты, функциональные заявления и предназначенным для ежедневного использования.

Аудиторы уделяют этим специфическим деталям, касающимся ухода за полостью рта, внимание на ранних этапах, и выявленные пробелы часто приводят к задержкам, перемаркировке или корректирующим действиям.
Пункты аудита, относящиеся к конкретной зубной пасте.
Зубные пасты подвергаются более тщательной проверке из-за заявлений об активных и лечебных свойствах.
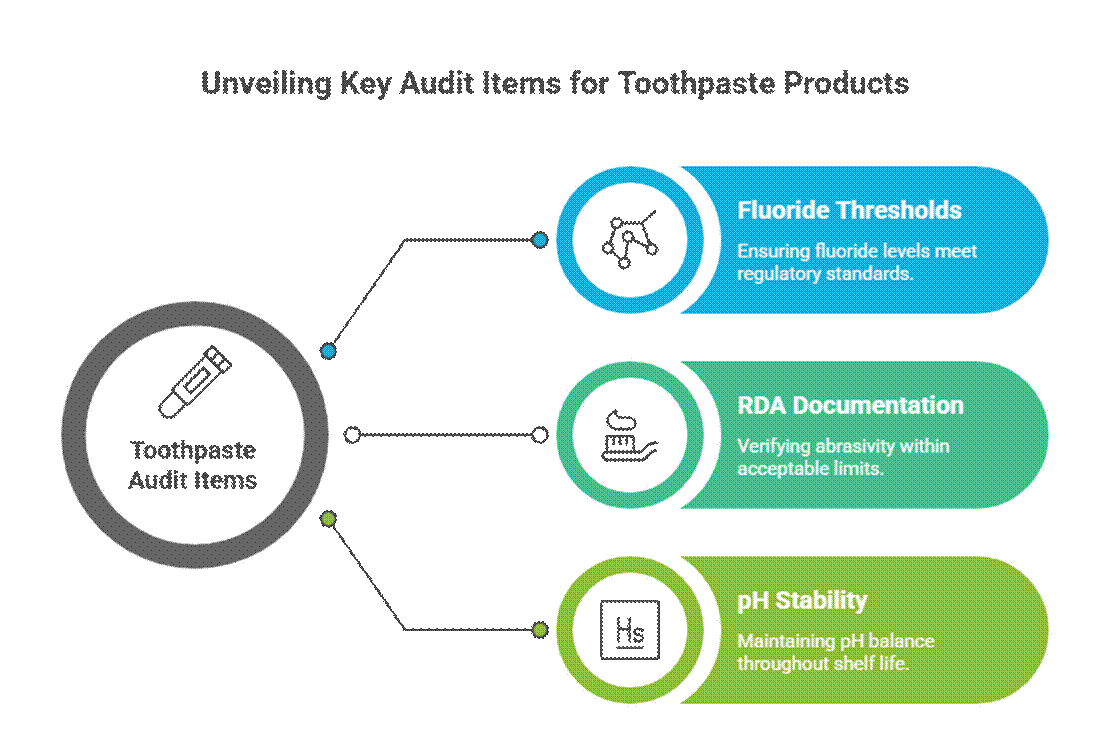
- Пороговые значения содержания фторида (актуально для монографии FDA)
В США, фторидная зубная паста Должна соответствовать монографии FDA о фторсодержащих зубных пастах, включая концентрацию активного вещества, формат маркировки и соответствие заявленным свойствам. Аудиторы также ожидают наличия документации о рекомендуемой суточной норме потребления (RDA) для зубной пасты и результатов подтвержденных испытаний на стабильность в течение всего срока годности.
- Документация RDA (пределы абразивности)
Аудиторы ожидают, что данные об относительной абразивности дентина (RDA) подтвердят безопасность эмали. Отсутствие или завышенные значения RDA являются распространенным тревожным сигналом, особенно для отбеливающих средств или средств на основе активированного угля.
- Стабильность pH в течение срока хранения
Уровень pH зубной пасты должен оставаться в безопасном, функциональном диапазоне на протяжении всего срока годности. Аудиторы проверяют данные о стабильности, чтобы убедиться, что изменение pH не снижает эффективность фтора или безопасность для полости рта.
Пункты аудита, касающиеся ополаскивателей для рта
Аудиты соответствия ополаскивателей для рта стандартам Особое внимание уделяется контролю микробов и концентрации активных веществ, особенно в формулах, требующих документации, подтверждающей соответствие требованиям CPC (Кодекса по контролю за продуктами питания и лекарствами), и тестирования эффективности консервантов.
- Классификация продуктов без алкоголя и продуктов, содержащих алкоголь
Зубные пасты подвергаются более тщательной проверке из-за заявлений об активных и лечебных свойствах.
- Документация CPC %
Аудиторы проверяют предельные концентрации и соответствие заявленным характеристикам формул, содержащих CPC.
- Отчеты о результатах микробиологических испытаний
Отсутствие или устаревшие результаты квалификационных тестов часто приводят к условному одобрению.
- Тестирование эффективности консервантов
Слабые консерванты рассматриваются как факторы, представляющие угрозу безопасности продукции.
Признаки опасности, связанные с отбеливающими средствами
Аудиторы тщательно изучают заявления регулирующих органов об отбеливающих зубных пастах, особенно формулировки, подразумевающие изменение эмали, стойкое отбеливание или терапевтические результаты, которые могут повлечь за собой надзор на уровне лекарственного средства.

- Заявления об отбеливающем эффекте против заявлений о лекарственном действии (США)
Утверждения, подразумевающие изменение эмали или терапевтические результаты, могут стать основанием для классификации препарата.
- Уведомление о наличии/отсутствии перекиси водорода
Аудиторы требуют четкого раскрытия информации об отбеливающих активных веществах и их концентрации.
- Формулировка заявления, которая влечет за собой проверку со стороны регулирующих органов.
Аудиторы требуют четкого раскрытия информации об отбеливающих активных веществах и их концентрации.
Вывод от производителя:
Аудиты средств по уходу за полостью рта терпят неудачу из-за активных ингредиентов и заявленных свойств, а не из-за эстетики упаковки.
Призыв к действию в середине статьи #1: Скачать образец пакета документов, подтверждающих соответствие требованиям.
Перед определением минимального объема заказа или окончательным выводом продукции на рынок ознакомьтесь с анонимизированной документацией OEM-производителя, готовой к аудиту.
Региональные системы аудита (ориентированные на исполнение)
Проверки различаются в зависимости от региона, но логика остается неизменной: регулирующие органы сначала оценивают риски, связанные с продукцией, затем документацию, и только потом маркировку. Различия заключаются в местах проведения проверок.
Соединенные Штаты — FDA и MoCRA
В США контроль за соблюдением законодательства все больше сосредотачивается на требованиях FDA к аудиту средств по уходу за полостью рта, при этом Соответствие требованиям MoCRA в области ухода за полостью рта Расширение ответственности производителей средств по уходу за полостью рта после выхода продукции на рынок.
- Схема принятия решения: косметические средства или безрецептурные препараты
Неправильная классификация является распространенным основанием для применения мер принуждения.
- Регистрация объекта и список продукции
Аудиторы проверяют точность регистрации в MoCRA и соответствие артикулов.
- Ведение протоколов партий и готовность к возникновению нежелательных явлений.
Бренды должны продемонстрировать наличие систем отслеживания происхождения продукции и обработки жалоб.
- Заявления об отбеливающих свойствах: где бренды переходят черту.
Преувеличенные заявления об отбеливающих свойствах часто вызывают пристальное внимание к лекарственным препаратам.
Европейский Союз — КПНП и ПИФ
Соответствие требованиям ЕС в отношении средств по уходу за полостью рта посредством CPNP и PIF требует полного согласования рецептуры, маркировки и требований CPSR для средств по уходу за полостью рта, при этом ответственность лежит на ответственном лице.

- Роль ответственного лица (ОП)
Ответственный за продукт должен контролировать и иметь доступ ко всему файлу с информацией о продукте.
- Ожидания от оценки безопасности
Регистрационные заявки на регистрацию лекарственных средств общего назначения (CPSR) часто отклоняются в отношении средств по уходу за полостью рта.
- Проверки на стабильность, соответствие требованиям CPSR и маркировку.
Несоответствия в документах — распространённые причины сбоев.
- Ответственность импортера
Ответственность лежит на импортере, а не на производителе оригинального оборудования.
Ближний Восток — GSO 1943
Регистрация GSO 1943 по уходу за полостью рта Это оказывает давление на таможенные органы, делая точность маркировки и единообразие при подаче документов критически важными для таможенного оформления грузов.
- Сроки регистрации продукции
Неполные заявки часто приводят к перезапуску процесса.
- Требования к маркировке на арабском языке
Отсутствие или некорректная арабская подзаголовочная маркировка часто приводит к задержке доставки.
- Распространенные причины конфискации товаров таможней
Изменения в маркировке после отправки заявки и несоответствия в документации.
Мелкий случай: задержка таможни ЕС вызвана несоответствием документации.
Европейский дистрибьютор импортировал отбеливающую зубную пасту с фтором, произведенную производителем оригинального оборудования низкого уровня. Хотя сама формула соответствовала требованиям, партия была задержана на таможне из-за несоответствий между информацией о продукте (PIF), данными о стабильности и окончательными заявлениями на этикетке. В отчете CPSR упоминалась более ранняя версия формулы; исследования стабильности в реальном времени не проводились, а заявленные отбеливающие свойства превышали то, что было одобрено экспертом по безопасности.
В результате товар был задержан таможней на четыре недели, потребовалась обязательная перемаркировка, а также возникли незапланированные расходы в размере 11 800 евро — при этом товарные запасы простаивали. Если бы версии рецептуры, протоколы стабильности и обоснование заявленных свойств были зафиксированы до подачи заявки, груз прошел бы таможенную очистку без вмешательства.
Именно поэтому опытные производители средств по уходу за полостью рта проводят параллельные испытания на стабильность, фиксируют версии рецептур до окончательной доработки PIF и проводят анализ рисков, связанных с заявлениями о побочных эффектах, до утверждения макета — предотвращая отклонения в документации, которые аудиторы немедленно выявляют.
Разъяснение ответственности
Строгое соответствие продукции производителей средств по уходу за полостью рта требованиям GMP, подкрепленное стандартом ISO 22716 для производства средств по уходу за полостью рта, гарантирует, что аудиторы смогут проверить соблюдение требований к отслеживаемости партий средств по уходу за полостью рта без корректирующих действий или отзывов продукции.
В Oralabx мы поддерживаем бренды, четко разграничивая юридическую ответственность и поддержку в реализации — предоставляя готовую к аудиту документацию по каждой партии, а также выявляя риски классификации и претензий до того, как они превратятся в проблемы с обеспечением соблюдения законодательства.
Ответственность импортера и производителя оригинального оборудования (раздел для разъяснения)
Четкое разделение ответственности имеет решающее значение для успешного прохождения проверок качества средств по уходу за полостью рта и предотвращения ответственности после выхода продукции на рынок. Регуляторы не оценивают “намерения” или неформальные договоренности — они оценивают, кто несет юридическую ответственность и кто контролирует документы. Когда роли неясны, контроль по умолчанию осуществляется импортером, даже если производитель оригинального оборудования (OEM) выполнил большую часть задач по обеспечению соответствия.
За что несет юридическую ответственность импортер
Независимо от поддержки со стороны производителя оригинального оборудования (OEM), регулирующие органы возлагают окончательную ответственность на сторону, выпускающую продукцию на рынок. Импортеры не могут передавать эти обязательства на аутсорсинг без явного юридического переуступления.

- Разрешение на продажу
Обеспечение получения всех необходимых разрешений до совершения сделки.
- одобрение заявок
Все маркетинговые заявления и утверждения на упаковке относятся к ответственности импортера.
- Сохранение розничной документации
Импортеры обязаны хранить и предоставлять по запросу документы, подтверждающие соответствие требованиям, включая доступ к PIF, сертификаты анализа, паспорта безопасности материалов и записи об отслеживаемости партий.
Что должен предоставлять компетентный производитель оригинального оборудования (OEM)
Квалифицированный производитель средств по уходу за полостью рта поддерживает соблюдение нормативных требований, предоставляя проверяемую, готовую к аудиту документацию, непосредственно связанную с каждой производственной партией.
- Сертификация GMP
Текущий, регионально признанная сертификация GMP (например, ISO 22716) демонстрирует системы контролируемого производства, гигиены и качества.
- Ведение учета партий и отслеживаемость
Полная документация по серийному производству, кодирование партий и отслеживание отзывов продукции, связывающее сырье, производственные циклы и готовую продукцию.
- Сертификат анализа (CoA), паспорт безопасности материала (SDS), отчеты о стабильности и микробиологической безопасности.
Сертификаты анализа, паспорта безопасности, исследования стабильности и отчеты о микробиологических/контрольных испытаниях, относящиеся к конкретной партии, должны соответствовать окончательной рецептуре.
- Экспорт документации
Точные коммерческие счета-фактуры, упаковочные листы, декларации и сопроводительные экспортные документы, соответствующие зарегистрированным данным о продукции и маркировке.
Визуальный заполнитель #2: Таблица ответственности импортера и производителя оригинального оборудования.
В этой таблице поясняется, как регулирующие органы распределяют ответственность во время проверок качества средств по уходу за полостью рта, а также где заканчивается поддержка со стороны производителей оригинального оборудования и начинается юридическая ответственность.
Ответственность импортера и производителя оригинального оборудования (соответствие стандартам в сфере средств по уходу за полостью рта)
| Область соответствия | Импортер (юридическая ответственность) | OEM (поддержка выполнения) |
| Классификация продукции | Окончательное решение о классификации | Ввод данных в рецептуру и индикаторы рисков |
| Разрешение на продажу | Регистрация, уведомление, назначение встречи по вопросам регистрации. | Подготовка данных и документов |
| одобрение заявок | Заявление о законности и обоснованности | Анализ страховых рисков и предоставление данных для поддержки |
| соответствие требованиям GMP | Проверяет соответствие требованиям OEM-производителя. | Обеспечивает функционирование систем надлежащей производственной практики (GMP) и проводит аудиты. |
| Прослеживаемость партий | Сохраняет и предоставляет записи. | Создает записи о партиях и коды партий. |
| Данные о стабильности и безопасности | Обеспечивает соответствие рыночным требованиям. | Проводит тестирование и составляет отчеты. |
| соответствие маркировки | Окончательное утверждение этикетки | Рекомендации по проверке и форматированию иллюстраций. |
| Готовность к аудиту розничной торговли | Сохранение документов | Предоставление и обновление документации. |
| Контроль и отзыв продукции | Финансовая и юридическая ответственность | Техническая поддержка расследований |
Ключевое уточнение:
Производители оригинального оборудования (OEM) обеспечивают соблюдение нормативных требований, но импортеры принимают на себя регуляторные риски, если ответственность не перекладывается по договору. Это различие имеет решающее значение для результатов аудита и рисков после выхода продукции на рынок.
Что на самом деле делает ХОРОШИЙ ОРГАНИЗАТОР ПРОИЗВОДСТВА АВТОМОБИЛЕЙ во время аудита
В РУКИГО, Аудиты не рассматриваются как документальные события. Наши команды OEM-производителей проектируют производственные системы с учетом нормативных контрольных точек с самого начала — внедряя отслеживаемость партий, активный контроль и проверку соответствия непосредственно в ежедневное производство.
Рабочий процесс обеспечения соответствия требованиям OEM (реальное исполнение)
В ходе аудита компетентные производители оригинального оборудования демонстрируют соответствие требованиям посредством контроля производственных процессов, а не путем реактивной документации. Аудиторы оценивают, интегрированы ли системы в повседневные производственные операции.
- Проверка рецептуры на лабораторном стенде
Перед масштабированием производства проводится валидация рецептур в лабораторных условиях для подтверждения концентрации активных веществ, диапазона pH и совместимости ингредиентов.
- Ускоренная работа + стабильность в реальном времени
Ускоренное тестирование стабильности позволяет подавать заявки на ранних этапах, а параллельные исследования в режиме реального времени позволяют подтвердить срок годности и выявить отклонения в составе.
- Создание партионной таблицы
Каждый производственный цикл сопровождается технологической картой, в которой указываются используемые материалы, параметры процесса, контроль качества на всех этапах производства и коды партий.
- Микробиологические и химические анализы
Готовая продукция проходит микробиологическое и химическое тестирование для подтверждения безопасности, эффективности консервантов и соответствия действующим веществам.
- Выпуск сертификата подлинности
Для каждой партии выдаются сертификаты анализа, которые перед выпуском сверяются со спецификациями.
- Экспортная и таможенная документация
Отгрузочные документы, декларации и файлы соответствия согласовываются с зарегистрированными данными о продукции во избежание таможенных расхождений.
Как терпят неудачу производители низшего уровня
Неудачи при проведении аудита часто объясняются системными недостатками, а не отдельными ошибками. Производители низшего уровня Как правило, у них отсутствует инфраструктура для обеспечения соответствия нормативным требованиям, и они реагируют только при возникновении проблем.
- Отсутствует отслеживаемость партии
Неполные или противоречивые данные о партиях продукции препятствуют эффективному отзыву продукции и немедленно подрывают доверие аудиторов.
- Повторное использование типового паспорта безопасности
Использование повторно выпущенных или не относящихся к конкретной партии паспортов безопасности (SDS) свидетельствует о плохом контроле качества рецептуры и часто выявляется в ходе проверок.
- Без проверки рисков по страховым случаям
Производители, которые не оценивают регуляторные риски, связанные с маркетинговыми заявлениями, подвергают бренды неправильной классификации и мерам принудительного исполнения.
- Реактивное (а не проактивное) соответствие
Соблюдение нормативных требований рассматривается скорее как запрос документов в последний момент, а не как интегрированная производственная система, что приводит к задержкам, корректирующим действиям и провалам аудитов.
Оригинальная коробка для еды на вынос:
Нарушения требований — это производственные сбои, а не проблемы с документацией. Аудиторы наказывают слабые системы, а не недостающие файлы.
В середине статьи CTA #2: Запрос на консультацию RP / MoCRA
Перед подачей документов в регулирующие органы или отгрузкой товара проконсультируйтесь со специалистом по вопросам соответствия требованиям, чтобы уточнить ответственность импортера, риски, связанные с классификацией продукции, и пробелы в документации.
Визуализация графика аудита (необязательно, но очень полезно)
Сроки проведения аудита различаются в зависимости от региона, но задержки неизменно возникают на одних и тех же этапах выполнения — решения по классификации, неполная документация и корректировка маркировки на поздних стадиях. Понимание того, где именно теряется время, позволяет брендам реалистично планировать запуск продукции и избегать блокировки товарных запасов.

Визуальный шаблон #3: Диаграмма хронологии аудита (США, ЕС и Ближний Восток)
Сравнение сроков проведения аудита ухода за полостью рта
| Этап аудита | Соединенные Штаты (FDA / MoCRA) | Европейский Союз (КПНП / ПИФ) | Ближний Восток (ГСО 1943) |
| Классификация продукции | Выбор между косметическими средствами и безрецептурными препаратами | Косметическая классификация | Косметическая классификация |
| Квалификация предприятия/производителя оригинального оборудования | Регистрация объекта | Сертификация OEM через RP | анализ данных OEM |
| Обзор безопасности и устойчивости | Ограниченный предрыночный период | CPSR + обзор стабильности | Обзор стабильности |
| Обзор заявлений и маркировки | Умеренный | Строгий, предрыночный | Строгий, предрыночный |
| Регистрация/уведомление | Список товаров | Уведомление CPNP | Регистрация продукта |
| Таможенное оформление | Контроль за соблюдением правил после выхода на рынок | Минимальный уровень загрязнения на границе. | Высокий уровень контроля |
| Выход на рынок | Ранний вход разрешен | Въезд после одобрения | Въезд после одобрения |
| Контроль за соблюдением правил после выхода на рынок | Высокий | Умеренный | Низкий-Умеренный |
Вывод от производителя:
Сокращение времени выхода на рынок достигается за счет параллельных процессов обеспечения соответствия требованиям, а не за счет пропуска этапов.
Заключение (закрытие сделки)
Долгосрочный успех в сфере ухода за полостью рта зависит от структурированных систем, а не от реактивной бумажной работы. Бренды, которые рассматривают аудит и соответствие продукции требованиям в области ухода за полостью рта как производственную дисциплину, а не как задачу по подаче документов, защищают прибыль, сроки и доверие розничных продавцов. Для брендов, масштабирующих выпуск зубной пасты, ополаскивателя для рта или отбеливающих средств, Oralabx выступает в качестве партнера по обеспечению соответствия требованиям — согласовывая рецептуру, документацию и системы управления партиями с реалиями аудита в США, ЕС и на Ближнем Востоке, чтобы получение разрешений регулирующих органов конвертировалось в предсказуемый доступ на рынок.
Часто задаваемые вопросы
В1. Кто несет юридическую ответственность в случае провала проверки качества средств по уходу за полостью рта — импортер или производитель оборудования?
Импортер по умолчанию несет юридическую ответственность. Производители оригинального оборудования могут поддерживать соблюдение нормативных требований, но ответственность перекладывается только в том случае, если она прямо переуступается договором и принимается регулирующими органами.
Вопрос 2. Требуется ли полная документация, подтверждающая соответствие требованиям для отдельных пакетиков с ополаскивателем для рта?
Да. Пакетики не являются исключением. Аудиторы оценивают состав, заявленные свойства и данные о безопасности независимо от размера упаковки.
Вопрос 3. Можно ли отправлять образцы ополаскивателя для рта в индивидуальной упаковке без паспорта безопасности или сертификата анализа?
В большинстве случаев — нет. Образцы могут перемещаться в ограниченном количестве случаев, но паспорт безопасности (SDS) и сертификат анализа (CoA) обычно требуются на таможне, особенно для жидких средств по уходу за полостью рта.
Вопрос 4. За сколько времени до запуска следует начинать работу по обеспечению соответствия требованиям?
В идеале, за 3–6 месяцев до запуска. Для продуктов с активными ингредиентами или отбеливающими свойствами планирование соответствия требованиям следует начинать еще раньше.
В5. Требуются ли для размещения товаров на Amazon сертификат подлинности (CoA) или паспорт безопасности (SDS)?
Amazon часто запрашивает сертификаты анализа (CoA), паспорта безопасности материалов (SDS) и документы, подтверждающие соответствие требованиям, во время утверждения объявлений или после проведения проверок, особенно для товаров для ухода за полостью рта.
Вопрос 6. Какие документы необходимо хранить на уровне розничного продавца?
Как правило, розничные продавцы по запросу требуют доступа к сертификатам анализа, паспортам безопасности материалов, записям об отслеживаемости партий и подтверждению разрешения на продажу.
Вопрос 7. Считаются ли заявления об отбеливающем эффекте заявлениями о лекарственном действии в США?
Да, могут. Заявления, подразумевающие необратимое отбеливание, изменение эмали или терапевтический эффект, часто вызывают пристальное внимание к лекарственным препаратам.
В8. Может ли ответственное лицо ЕС также работать на рынках стран Персидского залива?
Нет. На рынках стран Персидского залива требуются отдельные местные процедуры регистрации и соблюдения нормативных требований; регистрация в ЕС не распространяется автоматически на нормативные обязательства стран Ближнего Востока.
Окончательный призыв к действию: Контрольный список соответствия требованиям (PDF)
Избегайте задержек при проведении аудитов, расходов на перемаркировку и таможенных задержек.
Загрузите наш контрольный список по соблюдению правил гигиены полости рта в формате PDF или свяжитесь напрямую с нами. Специалист по соответствию стандартам OEM для проверки вашей документации перед запуском.






